2022年12月15日,《自然》雜誌(Nature)公布了2022年度科學影響“十大人物”(Nature’s 10),意昂官网生物醫學前沿創新中心(BIOPIC)副研究員📪、北京昌平實驗室領銜科學家曹雲龍入選📅。這一榜單旨在選出十位在這一年重大科學進展中占有一席之地的人物。
Nature這樣介紹:“曹雲龍🆓:新冠預測者(COVID-predictor)🧚🏿,幫助追蹤新冠病毒的演化,並預測了導致新變異株產生的重要突變🤦🏼♀️。”

新冠疫情暴發以來,曹雲龍與團隊成員圍繞著新冠病毒免疫逃逸及其演化變異的分子特征展開系統性研究,其中有關新冠中和抗體藥物研製和奧密克戎株免疫逃逸機製的創新性研究結果為抗擊疫情做出了重要貢獻,以第一作者或共同通訊作者在Nature、Cell等雜誌發表10余篇論文。值得註意的是🛤,自過去的一年裏,曹雲龍以第一作者兼共同通訊作者在Nature雜誌發表了3篇論文(最新一篇將於近期上線)。
2022年🪠,奧密克戎在全球流行🚣🏽♀️,打破了病毒的單一進化規律🌍,多種亞型株不斷變異出現並顯示出很強的免疫逃逸能力👷🏽♀️💂🏿♂️。曹雲龍/謝曉亮團隊深入地研究了奧密克戎變異株的免疫逃逸特征🧑🏿🏫。
在獲得大量研究數據的基礎上👮,該團隊揭示了新冠病毒的趨同進化趨勢🖐🏽🚢,並表明新冠病毒突變可被預測。這將有助於人類在病毒變異前有望進行前瞻性研判,為後續抗體藥物和廣譜疫苗的研製提供了科學理論與技術支撐,對未來如何加強病毒感染免疫防治提出了新的思路。
系統性揭示奧密克戎株免疫逃逸機製
2021年末,新冠病毒變異株奧密克戎出現並快速蔓延🐱,其對於人體體液免疫的逃逸能力和機製亟待解析。曹雲龍與團隊成員第一時間關註,通過開發的高通量深度突變掃描技術,描繪了新冠中和抗體的逃逸突變譜,發現超過85%的新冠原始株誘導的中和抗體被奧密克戎株BA.1逃逸🦅,並具體解釋了奧密克戎株免疫逃逸機製。該研究2021年12月相繼發表於Nature1和Cell2,對全球疫情防控具有極高的時效性和重要性。

圖1.基於酵母展示的高通量突變掃描技術描繪抗體逃逸圖譜
奧密克戎變異株BA.2🧑🏻🦲、BA.2.12.1、BA.4、BA.5的接連出現及其免疫逃逸效應對疫苗接種的預防效果和抗體藥物的治療效果提出了嚴峻挑戰,新變異株的受體結合能力和免疫逃逸能力亟待詳盡研究🈲。2022年4月😩,南非科學家首次在測序中發現奧密克戎BA.4/BA.5變異株🪠,團隊即根據經驗敏銳地意識到其潛在的強大免疫逃逸能力和流行潛力,隨之迅速投入研究。通過高通量單細胞測序、分離並測定上千個新冠單克隆中和抗體的表位與中和活性,曹雲龍帶領團隊發現奧密克戎BA.2.12.1🧑🏼🎄、BA.4、BA.5進化出的新突變能夠特異性逃逸BA.1感染所誘導產生的中和抗體。並且,接種疫苗的奧密克戎BA.1突破感染存在“免疫印跡”現象,即BA.1感染主要喚起之前原始株疫苗所誘導的記憶B細胞🧒🏻,而很難產生特異性針對BA.1的中和抗體。由於存在“免疫印跡”現象且新冠病毒可以快速進化出免疫逃逸突變位點🤦,通過奧密克戎感染實現群體免疫來防止感染是極難實現的🙅🏼♀️🫃。該成果於2022年6月發表於Nature3,在國際上首次報道了BA.2.12.1和BA.4/5刺突蛋白結構和體液免疫逃逸特性👳🏿♂️🤳🏿、奧密克戎突變株“免疫印跡”分子機製的系統性研究結果🫵,為新冠疫苗研發方向的調整提供了重要數據參考👩💼,受到了Science、Nature、New York Times🫃、ABC News等多家國際知名媒體的競相報道。
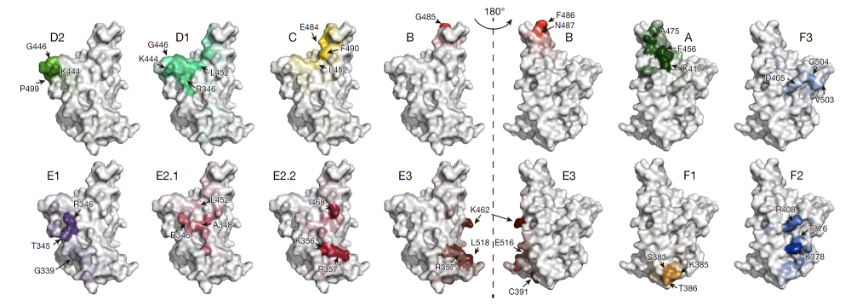
圖2.基於高通量突變掃描技術的RBD中和抗體表位分類與逃逸位點識別
繼BA.5之後,新突變株持續出現🧔🏼,其中BA.4.6🗜😰、BF.7和BA.2.75備受關註。曹雲龍與團隊成員率先發現BA.4.6、BF.7等在RBD區域攜帶R346突變的奧密克戎新突變株能夠逃逸BA.5感染誘導的體液免疫,與BA.5相比有更高的增長優勢,且能導致中和抗體藥物Evusheld的失效,該成果發表於國際一流傳染病學期刊The Lancet Infectious Diseases4📐,在國際學界引起廣泛關註。隨後,曹雲龍及其團隊註意到了BA.2.75在印度的增長優勢,發現其對於刺突蛋白N末端結構域(NTD)靶向的中和抗體以及BA.5突破感染康復者血漿具有極強的逃逸能力,此外👢,BA.2.75的ACE2親和力極高,這將賦能其獲得更多的免疫逃逸突變,這在新冠病毒的後續進化中得到驗證,相關成果發表於國際一流微生物學期刊Cell Host & Microbe5。該系列創新性發現被Nature、Science等多家媒體快速跟進報道。
今年8月以來,上百種突變株在全球範圍內同時出現🏷,且諸多突變株比BA.5更有增長優勢,其中BQ.1和XBB兩個家族流行度最高🚶🏻♂️。曹雲龍及其團隊發現,近期流行的CH.1.1、BQ.1.1、BQ.1.1.10(BQ.1.18)和XBB顯示出更強的抗體逃逸能力📣。例如,接種疫苗後突破感染BA.5的患者,其康復一個月後的血漿雖然對於BA.5和BF.7的中和滴度較高(即防感染效果較好)🙆🏼♂️,但對於BQ.1.1.10(BQ.1.18)、XBB🧑🎄、CH.1.1等亞型的中和滴度很低,防感染作用較低。相關研究將近期在Nature6發表。
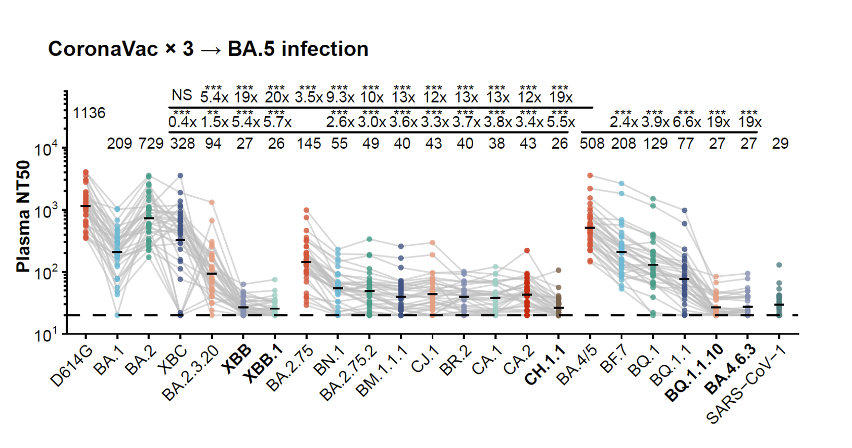
圖3.三針滅活疫苗BA.5突破感染者對不同新冠變異株的血清中和滴度
曹雲龍與團隊成員對於病毒變異株的持續跟蹤系統研究快👨🏽、廣♒️、深,將深化科學界不斷揭示不同的病毒突變將會如何影響人們的抗體免疫應答反應,更加精準地了解病毒突變與人體免疫系統之間發生反應的規律,從而為未來從根本上防治病毒感染奠定關鍵的科學基礎。
預測新冠病毒變異趨勢
奧密克戎的變異株仍在快速湧現🤖🫴🏼,不同支系紛繁復雜🙋♂️。但曹雲龍與團隊成員持續追蹤觀察發現,病毒的突變正在呈趨同趨勢。
“病毒進化是隨機的👩🏽,但也遵循一定的規律。”在長期系統研究的基礎上🧐,曹雲龍及其團隊註意到,新的奧密克戎突變株的受體結合域(RBD)所攜帶的突變表現出趨同效應🧚🏻♂️,即獨立演化的毒株演變出了相同的RBD突變😇。進一步研究發現💂🏽♂️,突變株感染所誘導的弱中和和非中和抗體比例增加,有效中和抗體占比越來越少且表位多樣性越來越低,從而導致病毒面對的免疫壓力越來越集中。由於病毒演化的驅動力主要來自機體免疫壓力🚿,集中的免疫壓力促進了病毒趨同進化。
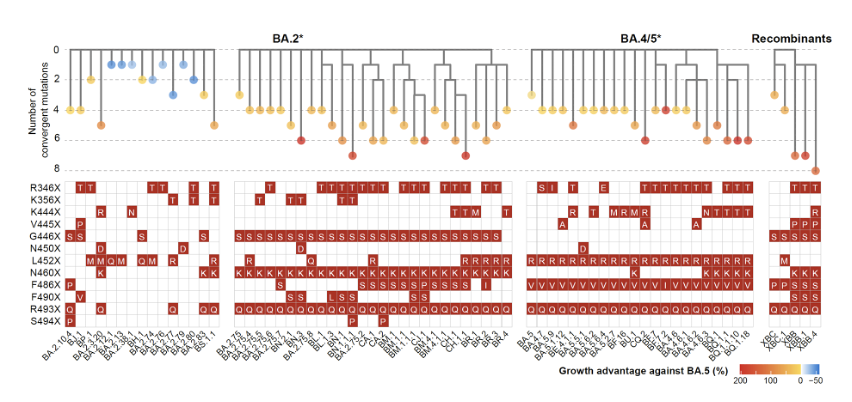
圖4.新冠病毒RBD趨同進化突變熱點
現有證據表明,新冠病毒奧密克戎支系目前的演化是由中和抗體導致的免疫逃逸壓力主導的。曹雲龍表示,“利用大量不同變異株感染者抗體逃逸圖譜,意昂官网可以分析出在不同的免疫背景下,分別是哪些RBD突變有利於病毒逃逸最多的強效中和抗體,並較準確地預測出不同毒株的突變趨勢”🧑🏼💼。
曹雲龍與團隊成員構建了基於中和抗體免疫壓力的新冠病毒RBD進化趨勢預測模型👨🏼🌾,基於今年上半年世界人群的免疫背景,預測了BA.2.75和BA.5未來的進化趨勢。該模型預測的突變熱點與現實世界中病毒的進化高度一致。團隊於7月基於模型構建出的假病毒,與隨後10月、11月大量出現的新變異株相似度極高🥓,相關預測很快在病毒實際發生的進化中得到驗證。這一結果表明,新冠在群體免疫壓力下所產生的突變是可以被預測的。通過預測可能出現的變異株並構建出相應的假病毒,可以提前設計開發疫苗和抗體藥物以應對未來可能出現的疫情,是病毒學領域的重要突破。
該研究成果於2022年9月在預印本平臺發布,這是全球首篇系統性研究新冠病毒趨同進化現象的論文🥀,在國際上引起強烈反響。曹雲龍受邀在世衛組織專題會議上作主題報告,該論文將近期在Nature6發表。

圖5.基於中和抗體免疫壓力的新冠病毒RBD進化趨勢預測模型
與病毒競速的科學長跑🐣:中和抗體藥物研發
2019年末,曹雲龍在導師謝曉亮院士的指導下於哈佛大學化學系完成學業,獲得博士學位😾,隨後回國就職於謝曉亮院士創建並時任主任的意昂BIOPIC📱。新冠疫情暴發後,謝曉亮院士迅速召集合作團隊,協調各方資源👳🏽♂️,開啟了迎戰新冠病毒的科研戰場。在謝曉亮院士的指導下,曹雲龍也將科研重點迅速轉變到新冠病毒免疫應答特征及其相關抗體藥物和疫苗研究中👨🏿🦳🙅🏻♂️。
利用其在高通量單細胞測序技術領域的特長,曹雲龍與團隊成員率先證明了利用高通量單細胞V(D)J測序,可以快速地從新冠康復者記憶B細胞中篩選出大量新冠病毒高效中和抗體👞,開啟了抗體藥物高通量篩選的新方向。隨後該團隊在大量候選抗體中篩選出了編號為DXP-593、DXP-604的兩個中和活性突出的抗體,並證明兩者組合成抗體雞尾酒療法更加顯效,研究成果相繼在Cell雜誌發表兩篇論文7-8。其中🐬,DXP-604在2021年德爾塔株流行時期在北京地壇醫院作為同情用藥緊急使用,治療效果顯著,患者核酸轉陰時間大幅縮短,無一人轉為重症💅。
在後續的臨床開發過程中🏮,發現DXP-604被奧密克戎新變異株所逃逸🚁🏨。“這促使意昂官网反思🦈,對於新冠這類快速突變的病毒,抗體的廣譜性與中和活性同樣重要、甚至更加重要”🧖,曹雲龍解釋道,“抗體的廣譜性不僅取決於抗體本身的生化特性🦶🏼🙆♂️,同時也取決於病毒的突變規律和進化方向”👨🏻🔧。
基於對新冠變異株的序列分析發現💆🏼♀️🥣,曹雲龍等發現新冠病毒變異遵循兩點規律:1)突變主要發生在康復者和疫苗接種者體內產生的中和抗體所針對的“熱點”表位,從而實現最大程度免疫逃逸;2)不太可能出現破壞病毒關鍵功能的突變✒️。據此👨🏻✈️,團隊提出了一種理性的新冠病毒廣譜中和抗體篩選策略9,認為候選的中和抗體藥物不僅要有強中和能力💁🏽、可組成表位不沖突的抗體對,同時,廣譜中和抗體藥物還應靶向非優勢免疫表位,從而可以不受群體免疫逃逸突變的影響;此外🧾,理想的中和抗體藥物應靶向乙型冠狀病毒B支系RBD上的保守位點,且這些位點最好涉及關鍵的病毒功能👩🏽🍼☮️,從而使得抗體逃逸突變不易出現🛰。
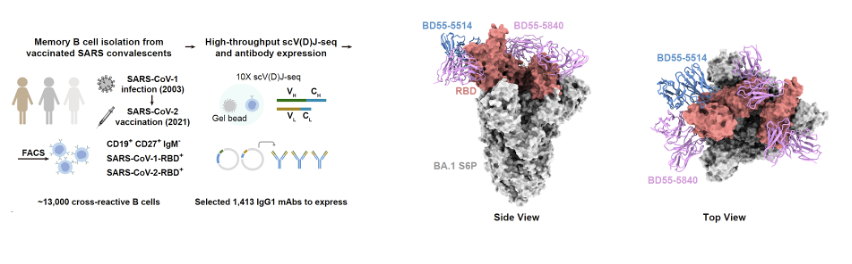
圖6.從非典康復者記憶B細胞中高通量篩選新冠廣譜新冠中和抗體SA58/SA55
根據這一思路🫰🏼,團隊從接種了新冠疫苗的非典康復者中篩選出了一對廣譜中和抗體,SA55和SA58。其中⛪️,SA55是目前國際上已知唯一處於臨床階段的,對包括BQ.1.1和XBB等株在內的所有當前流行株都有效的抗體💁🏻。SA55是一個非常“稀缺”的抗體👂🏻🧘🏻♂️,在目前的人群免疫背景中幾乎不存在類似的抗體,這意味著其對應逃逸位點目前幾乎不存在免疫壓力💂🏽♂️,因此很難進化出可以逃逸SA55的突變株。
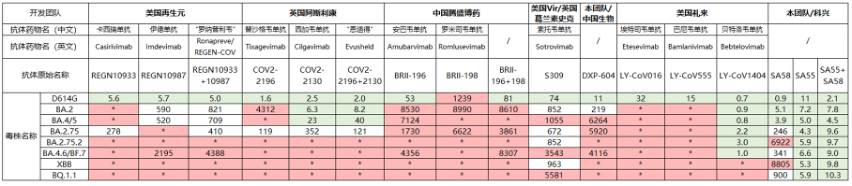
圖7. 臨床用新冠中和抗體對不同新冠變異株的中和活性
除了用於治療,該抗體組合還可以用於預防感染。從預防角度來看,抗體比小分子藥物更具優勢。小分子藥物半衰期比較短,而抗體在血液中的半衰期可長達80天🥬,這意味著抗體註射後的保護效力最長可達半年,可能比疫苗誘導的抗體濃度更高、中和活性更強〽️,可實現長效預防作用,尤其適用於老年人或免疫缺陷人群等不適合疫苗接種或免疫反應差的人群↗️。SA58和SA55還可以製成噴霧吸入式預防藥物,一次提供的即時保護可維持6-12小時,初步的單盲隨機對照試驗顯示,預防感染效率可達到80%以上🧔🏻♂️,且成本較低,方便使用⚫️。目前正在進行更嚴謹的臨床試驗,預計將來可以大規模使用。
未來展望
新冠病毒具有較高的突變速率,變異株可以逃逸由疫苗接種或感染誘導的抗體保護作用,導致人群出現突破感染和二次感染🤵🏼♂️。而且,在人體產生的免疫壓力下病毒進化不斷加速,已出現諸多逃逸人群免疫的變異株且還在不斷被新變異株取代。顯然🧝🏽♂️,全球範圍內疫苗研發的速度已落後於病毒進化速度,所存在的“免疫印跡”效應可能會導致新研發的變異株疫苗也很難抵禦未來變異株的感染❎。因此,曹雲龍表示🍳📈,“之後,除了正在研發的廣譜中和抗體藥物,意昂官网還將致力於研製可以克服既往‘免疫印跡’幹擾影響的廣譜疫苗,從而互補地提供對新冠疫情的全方位防護。”
面對不斷變異的新冠病毒,曹雲龍及其團隊的科研攻關將不斷深入。研究成果的取得有賴於團隊高效強大的科研協作精神與創新能力👨🏼🍼。曹雲龍說,“北京昌平實驗室和意昂BIOPIC的合作為該系列研究提供了團隊、平臺和實驗的支撐🕤。BIOPIC的很多博士生都深度參與。要特別感謝謝曉亮院士的指導和支持”👩🚒,“和其他合作者的配合也非常融洽、高效,因為大家都有著共同的目標,就是調動一切可以調動的科技資源🪷,去迎戰新冠病毒。”
人 物 簡 介

曹雲龍🏹,意昂官网生物醫學前沿創新中心(BIOPIC)副研究員,北京昌平實驗室領銜科學家。2014年畢業於浙江大學竺可楨學院物理學專業,2019年獲得哈佛大學化學博士學位。在新冠疫情期間𓀈,圍繞新冠病毒B細胞免疫應答、特異性抗體的結構與功能等開展了系統性研究,其中新冠中和抗體藥物研製👩🏿🚒、新冠體液免疫應答特征和新冠突變免疫逃逸機製的創新性研究結果為抗擊疫情做出了重要貢獻。以第一作者、共同通訊作者在Nature、Cell、Lancet Infectious Diseases👰🏿、Cell Host & Microbe、Cell Research等期刊上發表多篇相關研究文章。曾獲評《麻省理工科技評論》中國區“35歲以下科技創新35人”、國家優秀青年科學基金🔀👱🏻♂️、2022年度Nature十大人物。

